Présentation de la pharmacovigilance des "vaccins"
Statistiques pharmacovigilance française des "vaccins" Covid-19 au 1er juillet 2022
Quelques statistiques issues de ces données :
Rappel statistiques pharmacovigilance française des "vaccins" Covid-19 au 16 juin 2021
Quelques statistiques issues de ces données :
L’âge moyen au décès associé à la COVID19 est de 80 ans. L’âge moyen des myocardites associées au « vaccin » Pfizer est de 39 ans au 16/6/21
| Métrique | Pfizer | AstraZeneca | Moderna | Total |
|---|---|---|---|---|
| Nombre pages PDF | 2 487 | 1 698 | 413 | 4 598 |
| Taille fichier Excel fourni début août 2022 portant sur les cas jusqu'au 18/6/2021 | 1 804 ko | 1 225 ko | 320 ko | 4 349 ko |
| Nombre de cas pharmacovigilance | 27 617 | 19 677 | 4 628 | 51 922 |
| Nombre de lignes pharmacovigilance | 62 668 | 41 945 | 10 346 | 114 959 |
| Nombre de décès | 711 | 158 | 41 | 910 |
| Âge moyen au décès | 83.4 | 67.1 | 79.3 | 80.3 |
| Nombre de morts<=65 ans | 53 | 63 | 5 | 121 |
| Nombre de morts subites | 87 | 31 | 9 | 127 |
| Nombre de morts inexpliquées | 115 | 34 | 7 | 156 |
| Nombre de cas graves | 7 593 | 4 757 | 886 | 13 236 |
Explications
Principales pages du site
Page de recherche de cas de pharmacovigilance
Page d'accueil : extraits des principaux rapports d'analyse de la base de pharmacovigilance
D'où viennent ces données ?
Suite à une demande CADA du 17 avril 2021, l'ANSM a adressé le 9 août 2021, les cas anonymisés remontés jusqu'au 18 juin 2021 à 15h25 à la pharmcovigilance des "vaccins" Pfizer, Moderna et AstraZeneca sous forme de très gros PDF.
La dernière notification date du 16 juin 2021, mais il y avait 6 fois moins de notification ce jour là que 7 jours plus tôt ; idem pour les jours précédents ; il semble qu'il y ait des délais de plusieurs jours pour l'intégration des cas.
Le vaccin Jansen n'y figure pas car il n'avait pas été demandé en avril 2021.
Bien que l'ANSM ait envoyé des données en août 2021,
la CADA a été saisie quelques mois plus tard,
premièrement parce que l'on demandait aussi les enregistrements des réunions et deuxièmement au motif
que les données étaient au format PDF, ce qui n'est pas un format ouvert tel que prévu par la loi.
La CADA a émis un avis défavorable à la demande d'accès aux enregistrements
car ils n'existeraient pas alors que la loi le prévoit.
Mais la CADA a émis un avis favorable à la demande de transmission des données
dans un format ouvert tel que CSV, Excel ou XML.
L'ANSM a alors été relancé sur cette demande.
Début août 2022, l'ANSM a envoyé 3 fichiers Excel,
mais les cas s'arrêtaient à mi juin 2021 (avec quelques mises à jour par rapport au premier envoi).
On a aussitôt protesté auprès de l'ANSM rappelant les promesses de transparence de la directrice de l'ANSM
lors de son audition au parlement en vue de sa nomination.
On a rappelé que la demande portait sur des données depuis janvier 2021
et invoqué aussi de la jurisprudence sur la garantie d'accès aux données, dès lors qu'elles existent.
Enfin, On s'est engagé à respecter les recommandations de la CADA concernant le respect des droits des tiers
et la mise à disposition des données personnelles.
Ainsi le 13 août 2022, l'ANSM a envoyé 3 extractions Excel de la base de pharmacovigilance allant jusqu'au 1er juillet 2022.
A quoi correspondent les champs ?
Vous pouvez survoler l'entête des champs, vous aurez plus d'explications
Un document de l'ANSM explique la signification des champs
Les Champs C (Chronologie), S (Sémiologie) et B (bibliographie) sont des critères d'imputabilité utilisés en pharmacovigilance,
ils sont souvent suivi d'un chiffre, on peut trouver quelques explications ici
sur l'ancienne méthode Bégaud mais l'ANSM se réfère à une méthode actualisée
Y a t'il des précautions à prendre pour exploiter les données ?
Il s'agit de cas issus d'une base de données publique de pharmacovigilance.Le nombre de cas traditionnellement remontés à la pharmacovigilance est très bas, l'organisme VAERS américain estimait que le nombre de cas réels (y compris des décès) est à multiplier par 100.
D'autres sources disent que seuls 5 à 10 % des effets indésirables très graves sont remontés à la pharmacovigilance.
De multiples cas n'ont pas été investigués et l'on ne connait pas la suite de l'évolution du patient.
Les critères d'imputabilité sont évalués (quand ils le sont) de façon subjective et certains experts de la pharmacovilance ont des liens d'intérêts avec des laboratoires pharmaceutiques (voir les déclarations publiques d'intérêts de ces experts)
Pourquoi la pharmacovigilance peut elle être biaisée ?
Il suffit de comparer le grand écart entre l'imputabilité utilisée en pharmacovigilance et celui pour classifier un cas Covid pour voir l'étendue de la désinformation.
En effet, les morts comptabilisées comme associées à la COVID19 n'ont dans 30 % des cas eu aucun test sérologique, il y a juste eu une suspicion de COVID19 (ce qui suffit pour administrer du Rivotril, ce qui les achève).
De plus dans la très grande majorité des cas, la COVID19 n'est pas la seule cause de mortalité, mais plusieurs autres causes ont été mentionnées dans le certificat de décès.
Dans la pharmacovigilance, tout les prétextes sont bons pour écarter l'imputabilité d'un médicament : d'abord, si un effet se produit ou n'est constaté que longtemps après l'administration d'un médicament
(ce qui est le cas par exemple pour les problèmes de fertilité, cancer, fausses couches, malformations congénitales, dégénérescence neurologique...), il y aura de très grande sous notification car les personnes ne penseront pas à associer le médicament,
ensuite, les critères d'imputabilité seront défavorables pour établir un lien de causalité. A l'inverse, si l'effet se produit très vite, il sera souvent classifié comme "incompatible" !
Donc si certains disent qu'aucun effet indésirable d'un vaccin n'a été trouvé plus de 2 mois après sa mise sur le marché, ce qui est dans la réalité complètement faux,
c'est tout simplement parce que les méthodes de pharmacovigilance, de par leur conception même, écartent de tels effets à long terme.
Très peu d'autopsies ont lieu après une suspicion d'effet indésirable d'un médicament, si une autopsie prétend écarter le médicament, elle sera rendue publique immédiatement, dans le cas inverse, il faudra attendre des mois pour des "analyses complémentaires".
Le rôle partial de l'ANSM
Lors de l'état d'urgence sanitaire, l'état avait une responsabilité pécuniaire du fait des effets indésirables des vaccins.
C'est aussi le cas pour la vaccination obligatoire des soignants. L'ANSM, qui est une agence d'état a donc un intérêt à ce que l'état minimise sa responsbilité.
La campagne de vaccination étant organisée par l'Etat, l'agence d'Etat qu'est l'ANSM, placée sous la tutelle du ministère de la Santé ne met pas en avant
les risques associés aux médicaments préconisés par l'état, quoiqu'elle puisse évoquer, cachés au milieu de long documents de 50 pages, des signaux à l'étude.
L'ANSM a toujours eu un rôle partial lors de la crise sanitaire, on se souvient qu'au printemps 2020, elle menait ouvertement campagne contre l'hydroxychloroquine et appelaient ouvertement à ce que des cas de "mésusage" et de pharmacovigilance lui soit remontés, les morts de la COVID19
malgré un traitement tardif désespéré à l'hydroxychlororoquine remontaient dans la pharmacovogilance
alors même que les données historiques établissaient la sécurité de ce traitement.
Rappelons que légalement, une autorisation temporaire, telle que celle accordée aux vaccins, ne peut être délivrée que s'il n'existe pas d'alternative thérapeutique,
donc tout ceux qui promeuvent les vaccins ont intérêt à dénigrer les traitements précoces tels que l'hydoroxychloroquine+azithromycine+zinc, l'ivermectine, la vitameine D...
Par exemple, l'ivermectine n'a quasiment aucun effet indésirable, comparé aux vaccins qui provoquent très souvent des effets indésirables, plus ou moins graves.
Pourquoi y a t'il peu de cas jeunes ?
Concernant les données remontées jusqu'au 18 juin 2021, rappelons que l'accès la vaccination de 18 à 50 ans n'a été ouvert que le 31 mai 2021, avant cela seuls des soignants ou des personnes particulièrements vulnérables pouvaient se faire "vacciner".
Par ailleurs, le vaccin AstraZeneca a été interdit aux moins de 55 ans à partir du 19 mars 2021.
Les informations présentes ici sont elles fidèles ?
Lors de nos tests de cohérence, Nous n'avons pas perdu de données lors de la conversion du PDF pour l'extraire dans la base de données, seul le document PDF d'origine fait cependant foi et il convient de faire une recherche du cas dans le document PDF correspondant
La recherche en langage naturel prend en principe tous les critères de façon cumulative mais tous les cas de figure n'ont pas été testés.
Le nombre de lignes retournées étant limitées à 500, le dernier cas peut être tronqué.
Comment est caclulée la pValue ?
La pValue est calculée à l'aide d'une fonction Test Exact de Fisher que nous avons implémentée et qui fonctionne y compris pour des grands nombres.
Si la pValue est inférieure à 5%, on considère que les populations ne sont pas indépendantes, c'est à dire que l'intervention a un effet significatif. Ici, cela permet de voir su un "vaccin" produirait significativement plus d'effets indésirables qu'un autre.
A noter deux choses, sur la page Wikipedia sur le test exact de Fisher :
il est prétendu à la fin que le calcul de cette fonction sur des grands nombres est impossible, mais comme on ne savait pas que c'est impossible, on l'a fait quand même !
les statisticiens utilisent souvent le language/framework R pour calculer ce test mais le résultat retourné est souvent très approché, dans l'exemple donné par Wikipedia, R retourne pValue=0.002759 alors que Wikipedia dit que la bonne valeur est 0.001346... ! La fonction que nous avons implémentée retourne 0.0013460761879122351
Avez-vous des astuces pour la recherche ?
Il est possible de combiner plusieurs critères de recherche, par
exemple la recherche des décès avec un effet comprenant la chaîne "hépa".
Voir cette copie d'écran pour voir comment saisir cela
Du fait qu'un cas peut être stocké sur plusieurs lignes, la combinaison de plusieurs critères de recherche peut retourner des résultats inattendus.
La recherche en language naturel n'est pas sensible à la casse et aux accents, par contre le mot cherché doit être complet.
Par contre la recherche d'un effet cherche une partie du mot lorsqu'il fait entre 4 et 20 caractères,
par exemple la recherche sur l'effet 'cardie' retournera des lignes avec Tachycardie, Bradycardie, Tachycardie supraventriculaire etc..., elle n'est pas non plus sensible à la casse.
A quoi correspond le mode auto ?
Lorsque le nombre de lignes correspondant aux critères est supérieur ou égal à 500, un tableau avec des statistiques correspondantes (par vaccin, âge, gravité, évolution, plage d'âge)
est affiché afin de permettre d'affiner les critères
Droits informatique et libertés
Les données de pharmacovigilance étant issus d'un traitement de données automatisé d'informations personnelles,
elles peuvent être potentiellement considérées comme des données personnelles.
En effet, bien que nous ne connaissons pas les noms, prénoms, localisation des personnes concernées,
il est possible dans certains cas, de reconnaître les données d'une personne, notamment dans le cas où la personne concernée ou ses proches
ont médiatisé leur cas particulier marquant.
Dans certains cas, la personne concernée ou ses proches peuvent reconnaître la personne (par exemple si elles connaissent son âge et savent qu'elle a notifié tel jour tel effet indésirable
Vous pouvez exercer vos droits informatique et libertés (accès, rectification, opposition...) à l'adresse mail rgpd at consultation.bonsens.org
Cependant, comme les données à ma disposition sont totalement anonymes, si vous êtes concerné,
nous vous remercions d'indiquer précisément quel numéro de CAS vous concernerait car sinon, nous serions dans l'impossibilité de faire la relation.
en cas de contestation, vous pouvez vous adresser à la CNIL
Du fait de ces possibilités théoriques d'identification des victimes d'effets indésirables de vaccins et comme suggéré par les avis officiels, seules les statistiques sont affichées par défaut.
Pourquoi faut il s'identifier pour accéder aux données détaillées ?
Comme vu plus haut, les cas détaillés de pharmacovigilance, bien qu'anonymisés peuvent être considérées comme des données personnelles car dans certains cas, la personne concernée ou ses proches peuvent reconnaître la personne (par exemple si elles connaissent son âge et savent qu'elle a notifié tel jour tel effet indésirable).
Dans ce cas précis, la jurisprudence de la CADA permet d'accéder aux cas détaillés, pour les utilisateurs qui se sont identifiés.
L'identification se fait via la plateforme de consultation des adhérents de BonSens.org
Voici par exemple le début de la recherche détaillée sur le médicament Propanolol dans ce mode :
Nous avons masqué les dates de notification, numéros de cas et âges mais si vous êtes identifié, vous pourrez voir ces informations.
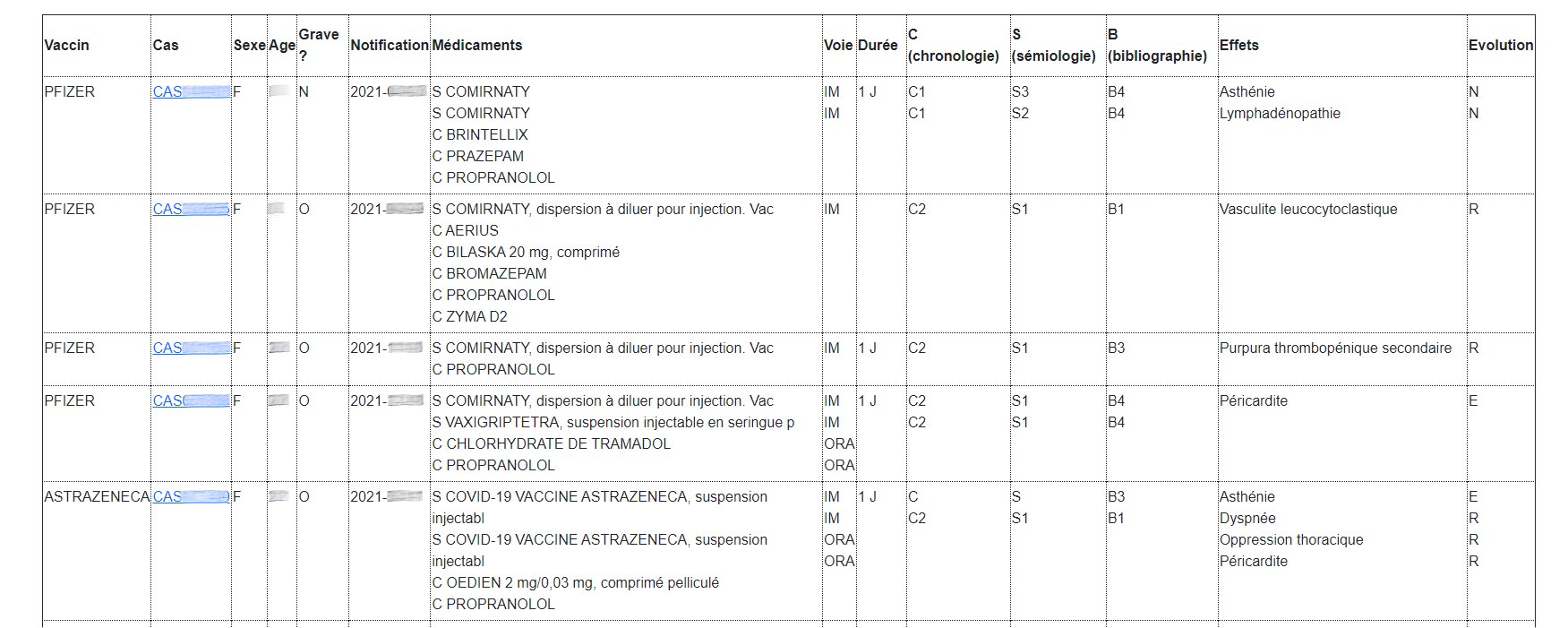
Ensuite si vous cliquez sur le 5ème cas (femme ayant eu notamment une péricardite suite à injection Pfizer), vous obtenez cette page de détail si vous êtes identifié :
(Là encore les champs ne seraient pas masqués)

La première section (détail du cas de pharmacovigilance pour le jeu de données 01072022) contient les décodages d'informations déjà présentes dans les résultats détaillés
La deuxième section (détail du cas de pharmacovigilance pour le jeu de données 18062021a) montre que ce cas là était déjà présent dans l'extraction des cas jusqu'au 18 juin 2021
mais que les évolutions étaient inconnues à ce moment là.
On peut noter également que 5 effets étaient initialement rapportés mais que l'un deux (une neutropénie) a mystérieusement disparu.
Le lien d'identification consultation des adhérents, se trouve également en bas de toutes les pages de ce site.
Les utilisateurs utilisant ce service doivent respecter les présentes règles, respecter les droits des tiers et s'abstenir notamment de diffuser publiquement des détails d'informations personnelles et traiter les éventuelles demandes informatiques et libertés.
Note : notre algorithme de correspondance des cas entre différents jeux de données n'est pas parfait mais trouve les bonnes relations, si elles existent, dans plus de 99% des cas
Interactions médicamenteuses des "vaccins" contre la COVID-19
Voir aussi les interactions médicamenteuses potentielles des vaccins Pfizer, Moderna, AstraZeneca
